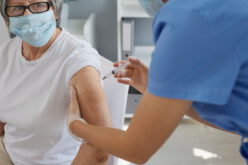
Antybiotyki to cudowna broń, ale nie na wszystko – rozmowa z prof. Walerią Hryniewicz
Lekarze za mało uczą się o diagnozowaniu zakażeń i właściwym stosowaniu antybiotyków Prof. Waleria Hryniewicz – konsultant krajowy w dziedzinie mikrobiologii lekarskiej Pani profesor, coraz częściej mówi się o rychłym nadejściu ery postantybiotykowej i straszy, że ludzie znów będą umierać z powodu chorób, które stały się wyleczalne po wynalezieniu antybiotyków. Czy to prawda, że drobnoustroje, z którymi jeszcze niedawno tak świetnie sobie radziliśmy, znów są dla nas groźne? – Tak, to prawda. Na skutek stosowania antybiotyków bakterie nabywają różnorodne mechanizmy oporności, a niewłaściwe, zwłaszcza nadmierne stosowanie antybiotyków powoduje przyśpieszenie tego procesu i sprzyja szybkiemu rozprzestrzenianiu się opornych szczepów bakterii. Potrafią one przekazywać nabyte geny oporności w sposób horyzontalny, to znaczy na plazmidach (cząsteczkach pozachromosomowego DNA występujących w cytoplazmie komórki, zdolnych do niezależnej replikacji), transpozonach (genach wędrujących), za pomocą fagów itp., i to nie tylko komórkom tego samego gatunku, ale także innym. Ze względu na coraz szerszą oporność na antybiotyki niewrażliwe na ich działanie szczepy bakterii przekazują jednocześnie „wiedzę” na temat szeregu grup tych leków, przez co stają się oporne na wiele antybiotyków, niekiedy na wszystkie dostępne w terapii. Które bakterie są dla nas obecnie największym zagrożeniem? – Jeśli weźmiemy pod uwagę praktykę pozaszpitalną, niewątpliwie najgroźniejsze są pneumokoki, nie bez powodu nazywane największymi zabójcami. To bakterie odpowiedzialne m.in. za ciężkie zapalenia płuc, sepsę, zapalenie opon mózgowo-rdzeniowych. W szpitalu największe zagrożenie stanowią pałeczki jelitowe wytwarzające enzymy – karbapenemazy, które są oporne na działanie grupy antybiotyków nazywanych lekami ostatniej szansy, czyli karbapenemy (np. ertapenem, imipenem, meropenem, doripenem). Są one zresztą zazwyczaj oporne na większość antybiotyków, które mogłyby być zastosowane w terapii zakażeń przez nie wywoływanych. Kolejny poważny problem to gronkowce złociste oporne na metycylinę, z którymi mamy do czynienia w praktyce pozaszpitalnej i weterynarii – u zwierząt hodowlanych. Jak widać, rezerwuar antybiotykoopornych bakterii jest ogromny. Czy to prawda, że szpitale są siedliskiem najgroźniejszych szczepów bakterii? W jaki sposób można z nimi walczyć? – Szpital jest miejscem szczególnym. Przebywający w nim chorzy często mają wiele czynników ryzyka sprzyjających zakażeniu. Częste hospitalizacje, np. pacjentów z przewlekłymi chorobami czy pensjonariuszy domów opieki długoterminowej, a także inwazyjne procedury diagnostyczno-terapeutyczne sprzyjają zakażeniom wywoływanym przez bakterie antybiotykooporne. W ostatnim czasie obserwuje się zawlekanie tego typu bakterii z innych części świata, zarówno z krajów rozwiniętych, jak i rozwijających się, czemu sprzyjają nasza mobilność, wymiana handlowa oraz intensywne migracje ludzi. Rozprzestrzenianie się tych niebezpiecznych patogenów coraz częściej jest widoczne również w Polsce. Od 2008 r. obserwujemy szybkie rozprzestrzenianie się szczepów Klebsiella pneumoniae wytwarzających karbapenemazy, a w ostatnim czasie szczególnie dynamicznie szerzy się Klebsiella pneumoniae wytwarzająca karbapenemazę NDM (od New Delhi). Metody biologii molekularnej często pozwalają nam ustalić, skąd one pochodzą. Aby ograniczyć niebezpieczeństwo przedostawania się tych opornych szczepów bakterii do szpitali, konieczne jest zbadanie na ich nosicielstwo pacjentów przyjmowanych z innych placówek medycznych, i to zarówno z kraju, jak i z zagranicy. W przypadku identyfikacji niebezpiecznych bakterii możemy podjąć działania mające na celu zapobieżenie rozprzestrzenieniu się ich w szpitalu. W tej sprawie została wydana rekomendacja podpisana przez ministra zdrowia. Od wielu lat apeluje pani do środowiska lekarskiego, aby z umiarem i rozsądkiem przepisywało antybiotyki. Czy te apele i opracowany pod pani kierownictwem przez największe polskie autorytety medyczne Narodowy Program Ochrony Antybiotyków przyniosły oczekiwany skutek? – Niestety, jeszcze nie, ale powoli dociera do naszej świadomości to niebezpieczne zjawisko, którego ofiarą może być każdy z nas. Opracowywane rekomendacje są coraz częściej wykorzystywane przez lekarzy w szpitalach, zwłaszcza na oddziałach intensywnej terapii, gdzie antybiotykooporność stanowi bezpośrednie zagrożenie dla zdrowia i życia pacjentów. Niestety, w podstawowej opiece zdrowotnej jest gorzej – ciągle zbyt często przepisuje się antybiotyk „na wszelki wypadek”, a także na zakażenia wirusowe. Dlaczego nie powinno się stosować antybiotyków w leczeniu chorób o podłożu wirusowym, np. grypy? A może są już jakieś odstępstwa od tej reguły? – Antybiotyki nie działają na wirusy, a jak każdy inny lek mogą wywoływać działania niepożądane, niekiedy nawet bardzo ciężkie, np. uszkodzenie wątroby, neurotoksyczność,