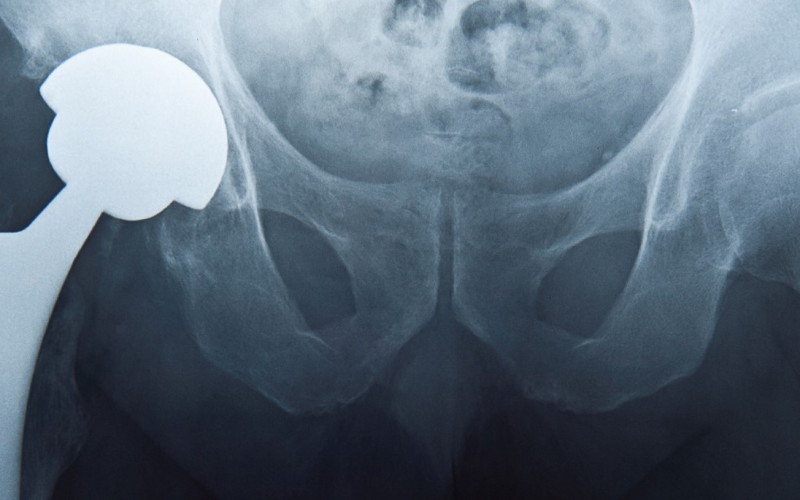
Proszę o telefoniczne uzgodnienie terminu wizyty w moim gabinecie w celu dokonania oceny stanu Pani/Pana endoprotezy stawu biodrowego. Podczas tej wizyty chciałbym omówić z Panią/Panem ewentualne niepokojące objawy/problemy, wykonać dodatkowe zalecone badania i ustalić najlepszy plan badań i dalszego leczenia. Koszty badań i wizyt kontrolnych pokryje firma DePuy, jak opisano w załączonym dokumencie »Informacje dla pacjentów«. (…). Wszelkie pytania dotyczące działania implantu proszę kierować do mojego gabinetu. Odpowiedzi na pytania dotyczące opłat za leczenie można uzyskać, dzwoniąc do DePuy, pod numer telefonu zamieszczony w dokumencie »Informacje dla pacjenta« (…).
W załączeniu do niniejszego listu przesyłam również »Formularz zgody pacjenta«. Wypełnienie tego formularza umożliwi mi udostępnienie informacji związanych z Pani/Pana protezą stawu biodrowego firmie DePuy, a także innym stronom działającym w jej imieniu. Informacje te są niezbędne do ustalenia, czy jeden z wycofanych produktów został wszczepiony w Pani/Pana przypadku oraz czy poniesione koszty leczenia podlegają zwrotowi (…)”.
Bez paniki, ale…
Z treści przygotowanego przez firmę listu do pacjentów wynika, że podpisać się pod nim powinien ortopeda, który wykonał operację wszczepienia endoprotezy, albo szpital, gdzie ją przeprowadzono. Jednak dzisiaj, po pięciu latach od przesłania tego listu przez DePuy, okazuje się, że liczni polscy pacjenci z endoprotezami uznanymi za wadliwe go nie otrzymali i trudno dociec, czy w ogóle został do kogokolwiek wysłany. Nie wiedzą zatem, że w ich ciele tkwi proteza, która może szkodzić zdrowiu, a jeśli odczuwają jakieś dolegliwości, nie zdają sobie sprawy dlaczego. Nie zostali powiadomieni, jakie objawy powinny ich niepokoić i jak mają dalej postępować, chociaż Brytyjska Agencja Leków i Produktów Leczniczych 22 kwietnia i 22 maja 2010 r. informowała, że powinni zostać zdiagnozowani klinicznie i poddani badaniom radiologicznym. Można przypuszczać, że niektórym pacjentom już wymieniono tę endoprotezę, bo niezależnie od rodzaju implantu przeprowadza się pewien procent reoperacji, ale nadal nie wiedzą oni, że wcześniej powinni być objęci badaniami kontrolnymi. Koszty ich leczenia i reoperacji pewnie pokrył NFZ, choć można było otrzymać te kwoty od firmy DePuy. Ortopedzi, którzy wszczepiali te endoprotezy, twierdzą, że wysłanie listu skierowanego przez DePuy do pacjentów nie należało do ich obowiązków. W ogóle niechętnie rozmawiają na ten temat, zasłaniając się brakiem uregulowań prawnych, które by ich do tego zobowiązywały. A względy moralne? Medyczne? Można wnosić, że takie chyba już nie istnieją.
Niektórzy ortopedzi byli zdania, że nie należy niepokoić osób mających te endoprotezy, skoro nie doświadczają żadnych dolegliwości, bo gdyby je odczuwały, zgłosiłyby się do szpitala, gdzie wszczepiono implant. Dodawali zwykle, że endoprotezy tej firmy są na ogół dobre i większość nigdy nie będzie sprawiać swoim właścicielom problemów zdrowotnych, a komplikacje i konieczność reoperacji mogą zaistnieć zawsze, niezależnie od rodzaju produktu. Żaden lekarz, z którym rozmawiałam, nie chciał jednak oficjalnie wypowiedzieć się w tej sprawie.
Nie należy siać paniki, ale skoro producent zaleca objęcie kontrolą osób, którym wszczepiono te endoprotezy, widocznie jest to wskazane i pacjenci powinni o tym wiedzieć.
Lista zlekceważonych badań
Co proponowała firma? Jeśli po badaniu klinicznym chirurg lub pacjent są zaniepokojeni stanem biodra, zalecane są następujące badania:
• Krwi na obecność kobaltu i chromu. Poziom stężenia jonów kobaltu i chromu nie powinien przekraczać 7 mg/l.
• Gdy okaże się, że stężenie któregoś z tych pierwiastków jest wyższe, a nie wystąpiły inne objawy – po trzech miesiącach trzeba to badanie powtórzyć.
• Jeśli powtórne badanie potwierdzi, że poziom tych pierwiastków jest podwyższony, trzeba rozważyć wykonanie rezonansu magnetycznego lub USG. Natomiast gdy lekarz stwierdzi odczyn zapalny tkanek miękkich, gromadzenie się płynu lub narastanie tkanki, musi wziąć pod uwagę konieczność przeprowadzenia operacji rewizyjnej.
Wyniki, które należy uznać za niepokojące:
• podwyższony poziom metali we krwi, głównie kobaltu i chromu,
• złe ustawienie panewki, obluzowanie endoprotezy,
• guz rzekomy i ból w obrębie miejsca operacji uniemożliwiający z czasem chodzenie.
Jeśli zaś poziom jonów metali będzie niższy niż 7 mg/l i/lub wyniki rezonansu magnetycznego albo USG pozostaną w normie, należy poddawać pacjenta corocznym badaniom przez pięć lat od wszczepienia protezy.
Nie ma w tych propozycjach zaleceń podejmowania szybkich, radykalnych rozwiązań, są tylko wskazania do kontroli pacjentów, i to przez wiele lat.
Najczęstsze objawy, które mogą świadczyć o szkodliwym działaniu tej endoprotezy, to ból, obluzowanie lub przesunięcie implantu, wrażliwość na metale, zakażenie, złamanie kości. W pierwszym okresie po zabiegu pacjenci mogą nie odczuwać dolegliwości, dopiero z czasem pojawia się ból i opuchnięcie w okolicach stawów. Mogą też zostać uszkodzone niektóre mięśnie, kości i nerwy w okolicy biodra z wszczepionym implantem.
Porażka firmy DePuy wywołała na świecie falę dyskusji nad jakością endoprotez metalowych, które wielu doświadczonych ortopedów uważa za najtrwalsze. Wiadomo jednak, że nie mogą być one stosowane u osób uczulonych na metal, z którego wykonane są implanty. Niekiedy też uwalniające się z nich do organizmu jony kobaltu, chromu lub niklu mogą się okazać szkodliwe.
Ministerstwo nie widzi problemu
W Polsce o endoprotezach uznanych pięć lat temu za wadliwe cicho. Zwróciłam się więc do Ministerstwa Zdrowia z listą pytań: Ilu pacjentom wszczepiono u nas w latach 2003- 2010 endoprotezy firmy DePuy uznane potem za wadliwe? Czy zostali o tym powiadomieni? Czy otrzymali list, który przygotował dla nich producent? Jaka jest sytuacja zdrowotna tych pacjentów? Czy któryś z nich choruje na kobaltozę? Gdzie mogą wykonać badania określające poziom kobaltu, chromu czy niklu we krwi?
Odpowiedź, którą otrzymałam, jest bardzo ogólnikowa. Została oparta na informacjach konsultanta krajowego w dziedzinie ortopedii i traumatologii narządu ruchu prof. dr. hab. n. med. Pawła Małdyka oraz Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych. Przyznano w niej: „W Polsce firma rozesłała informacje do wszystkich ośrodków, które stosowały tę endoprotezę, z zaleceniem dla chorych zarejestrowania się w wyznaczonej firmie prawniczej, która miała reprezentować producenta endoprotez”. Napisano też, że „w listopadzie 2012 r., pod auspicjami konsultanta krajowego w dziedzinie ortopedii i traumatologii narządu ruchu – prof. Pawła Małdyka, odbyła się konferencja użytkowników endoprotez resurfacyjnych, podczas której nie zgłoszono istotnych powikłań związanych z tym typem endoprotezy u pacjentów na terenie kraju. Wskazano na potrzebę monitorowania tych chorych i w miarę możliwości badania poziomu metali ciężkich – kobalt, chrom w surowicy i moczu”.
Czy wymienione wskazania i zalecenia zostały wypełnione? Nie wiadomo, ministerstwo na ten temat milczy. Dziwne wydaje się też to, że endoprotezy uznane przez samego producenta za wadliwe u nas nie powodują istotnych powikłań.
Można się ubiegać o zadośćuczynienie
Jak powinien postępować w tej sytuacji polski pacjent mający wadliwą endoprotezę firmy DePuy? Z tym pytaniem zwróciłam się do mec. Jolanty Budzowskiej, która od lat z dobrym skutkiem dochodzi roszczeń odszkodowawczych pacjentów, w tym związanych z wadliwymi protezami stawu biodrowego.
– Polski pacjent powinien przede wszystkim zgłosić się do lekarza ortopedy – najlepiej tego, który przeprowadzał zabieg wszczepienia endoprotezy, z prośbą o przeprowadzenie lub zlecenie podstawowej diagnostyki. W grę wchodzą w tym przypadku szczególnie badania krwi pod kątem stężenia kobaltu i chromu, ponadto badania obrazowe operowanego stawu biodrowego. Jeżeli wyniki badań, zwłaszcza laboratoryjnych, nie będą prawidłowe, należy porozmawiać z lekarzem o zasadności przeprowadzenia operacji rewizyjnej endoprotezoplastyki stawu biodrowego. Każdy pacjent z tego typu endoprotezą powinien być zainteresowany przeprowadzeniem diagnostyki – nawet jeżeli nie dokuczają mu żadne konkretne dolegliwości. Zdarzało się, że pacjenci nieodczuwający dolegliwości mieli przekroczone normy kobaltu i chromu we krwi, co może nieść ze sobą poważne ryzyko. Niestety, prawdą jest, że wielu pacjentów nie jest informowanych przez swoich lekarzy o konieczności diagnostyki; spora grupa nie wie nawet, jaki model endoprotezy im wszczepiono. Każdy pacjent może się zwrócić do szpitala, w którym endoproteza była wszczepiana, o wydanie kserokopii pełnej dokumentacji medycznej. W tej dokumentacji należy zwrócić szczególną uwagę na tzw. metryczki endoprotezy, z których w sposób jasny wynika, jaki model został użyty podczas operacji. Jeżeli wyniki badań okażą się nieprawidłowe, a w szczególności jeżeli pacjentowi zalecana jest powtórna operacja stawu biodrowego, powinien rozważyć ubieganie się o zadośćuczynienie od producenta endoprotez.
35 tys. endoprotez
Co roku wszczepia się w kraju ok 35 tys. endoprotez stawu biodrowego. Na Zachodzie operacji tych jest znacznie więcej. Pozwalają one chorym odzyskać pełną sprawność. Zdarzają się jednak powikłania, ale producenci, analizując je, ciągle udoskonalają swoje endoprotezy. W Wielkiej Brytanii zaleca się, by wszyscy pacjenci z metalowymi endoprotezami poddawali się co roku badaniom poziomu kobaltu i chromu.
Kobalt i chrom
Kobalt jest niezbędny do życia, wchodzi w skład witaminy B12 – kobalaminy, wpływa na produkcję szpiku kostnego i czerwonych krwinek. Znane są objawy zatrucia kobaltem: białko w moczu, biegunka, drgawki, duszność, krwiomocz, łzawienie, niepokój, spadek ciśnienia, uszkodzenie serca, zżółknięcie skóry, żółtaczka. Natomiast zatrucie chromem objawia się zapaleniem żołądka, jelit, bólami brzucha, nudnościami, wymiotami, biegunką, zatrzymaniem moczu, uszkodzeniem nerek, mocznicą. Metaloza jako choroba występuje zwykle na skutek pracy w warunkach szkodliwych, Instytut Medycyny Pracy wykonuje więc badania na obecność tych pierwiastków w organizmie.
Strony: 1 2
















Proszę Pani, firma DePuy nie poinformowała pacjentów o tym, że wypuściła wadliwe protezy! Być może poinformowane zostały szpitale, natomiast nie przekazały one informacji pacjentom. Bliska mi osoba przeszła przez wieloletnie piekło zanim udało jej się dociec, że winowajcą jest starta niemal do zera metalowa proteza! Zgroza! Informację o wadliwej protezie otrzymała dopiero po reoperacji!!
witam. Moja mama właśnie wczoraj przeszła operację wymianę o to tej właśnie protezy je poziom kobaltu i chromu był 120 razy większy niż powinien. Gdzie ubiegać się o odszkodowanie,do kogo się zgłosić ?
Gdzie mozna to zbadac iile kosztuje?
oj tam poziom irydu jest ważny
Pani Aniu zapraszam do kontaktu – ffilipp@op.pl