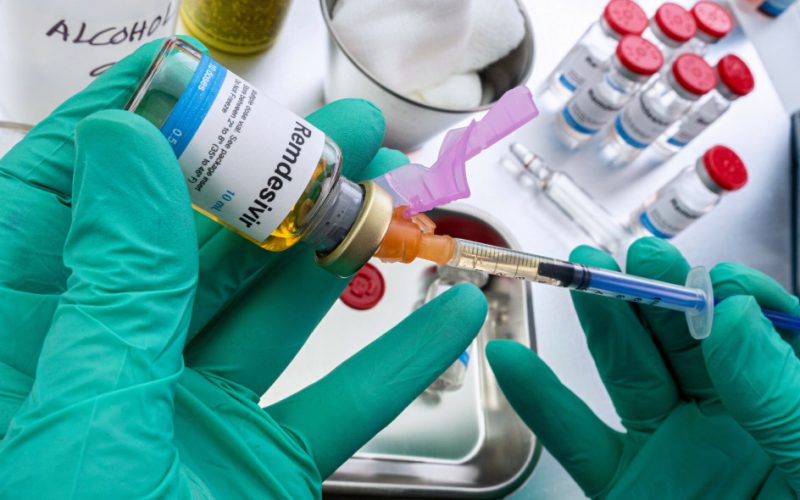
Już w grudniu w USA może się pojawić pierwszy, powszechnie dostępny lek na COVID-19 Rok temu opisaliśmy na łamach PRZEGLĄDU rywalizację koncernów farmaceutycznych pracujących nad szczepionką przeciw COVID-19. Na czele stawki była wówczas AstraZeneca współpracująca z zespołem naukowców Uniwersytetu Oksfordzkiego. Po piętach deptały jej dwie amerykańskie firmy – Moderna z własną szczepionką oraz Pfizer z preparatem opracowanym przez niemiecką spółkę BioNTech. Wiosną dołączył koncern Johnson & Johnson ze szczepionką jednodawkową. W Europie i Stanach Zjednoczonych te cztery specyfiki stały się podstawowym orężem w walce z pandemią. Dziś celem branży farmaceutycznej jest wprowadzenie na rynek skutecznego leku na COVID-19, bo kolejne fale zachorowań pojawiają się nawet w krajach, w których odsetek zaszczepionych obywateli jest bardzo wysoki, takich jak Izrael czy Singapur. Zdarza się też, że organizm osoby zaszczepionej reaguje niedostatecznie, co prowadzi do przykrych konsekwencji. Dlatego potrzebny jest lek, który zapobiegałby konieczności hospitalizacji pacjentów będących w najwcześniejszych stadiach choroby. Blisko, coraz bliżej… Lekarze w bogatych krajach mają już do dyspozycji przeciwciała monoklonalne, które podawane są dożylnie w szpitalach i na ogół okazują się skuteczne. Lecz to za mało. By pokonać pandemię, potrzebne są też powszechnie dostępne i możliwie niedrogie leki. Amerykańskie media wymieniają dziś trzy koncerny, które są najbliżej uzyskania rejestracji swoich specyfików przez Agencję Żywności i Leków i wprowadzenia ich na rynek. To Merck & Co., Pfizer Inc. i F. Hoffmann-La Roche AG. Przy czym należy zaznaczyć, że już 22 października 2020 r. w Stanach Zjednoczonych został zatwierdzony do stosowania w warunkach szpitalnych pierwszy lek przeciw COVID-19, remdesivir, produkowany przez firmę Gilead Sciences Inc. Opracowano go z myślą o leczeniu eboli, lecz nie spełnił pokładanych w nim nadziei i nie uzyskał rejestracji. Rok temu okazało się, że może być skuteczny w leczeniu pacjentów z ciężkim przebiegiem COVID-19. Przyśpieszał ich powrót do zdrowia, choć nie wykazano, by zmniejszał liczbę zgonów. W połowie ubiegłego roku Europejska Agencja Leków zezwoliła na stosowanie remdesiviru na naszym kontynencie. Także polska Agencja Oceny Technologii Medycznych i Taryfikacji zaleca stosowanie go u pacjentów z potwierdzonym zakażeniem SARS-CoV-2 w okresie replikacji wirusa, czyli nie później niż pięć-siedem dni od wystąpienia pierwszych objawów choroby. Pod kątem skuteczności w zwalczaniu SARS-CoV-2 badane były również inne stosowane już leki, co czasem prowadziło do poważnych kontrowersji. W czerwcu 2020 r. australijscy naukowcy ogłosili, że Iwermektyna – lek zwalczający choroby pasożytnicze u zwierząt i ludzi – we wstępnej fazie badań prowadzonych w warunkach laboratoryjnych znacznie osłabił oddziaływanie koronawirusa. Tyle wystarczyło, by zaczął być postrzegany jako cudowny lek na covid. Późniejsze badania tego nie potwierdziły, jednak Iwermektyna zyskała sporą popularność. Podobnie rzecz się miała z amantadyną. Dziś i ten specyfik nie jest zalecany w leczeniu covidu. Rywalizacja gigantów Specyfikiem, który może wiele zmienić, jest molnupiravir, produkowany przez koncern Merck & Co. Jego historia zaczęła się, gdy mało kto na świecie zdawał sobie sprawę z zagrożenia, jakie niósł SARS-CoV-2. W styczniu 2020 r., w trakcie zorganizowanej w San Francisco konferencji poświęconej opiece zdrowotnej, dr George Painter – prezes Emory Institute for Drug Development z Atlanty, i Wendy Holman – dyrektor generalna spółki Ridgeback Biotherapeutics z Miami, dyskutowali o tym specyfiku, nad którym badania były kontynuowane dzięki finansowemu wsparciu z Narodowego Instytutu Zdrowia. Dr Painter uważał, że molnupiravir może się okazać skuteczny w leczeniu grypy, Wendy Holman była zaś ciekawa, czy nadaje się do zwalczania eboli. Oboje zgodzili się, że molnupiravir ma tak szerokie spektrum działania, że może być skuteczny przeciwko wielu chorobom. Ostatecznie w drugiej połowie marca 2020 r. firma Ridgeback Biotherapeutics zakupiła technologię produkcji molnupiraviru, a miesiąc później miała już umowę z farmaceutycznym gigantem, koncernem Merck & Co., który od lat zajmował się badaniami nad wirusami HIV i eboli. Pierwsza faza badań klinicznych ruszyła jesienią 2020 r. Dziś kończy się III faza badań i wkrótce koncern będzie dysponował opracowanymi wynikami. Jeśli uda się wykazać, że molnupiravir jest skuteczny i bezpieczny dla pacjentów, zostanie on zarejestrowany i trafi na rynek. Będzie to wielki sukces
Tagi:
apteki, AstraZeneca, Atea Pharmaceuticals, biologia, Biomed Lublin, BioNTech, biotechnologia, Biotechnology Innovation Organization, Chugai Pharmaceutical, F. Hoffmann-La Roche AG, Fujifilm Holdings, George Painter, Gilead Sciences Inc., iwermektyna, Izrael, Johnson & Johnson, lekarstwa, lekarze, Pfizer Inc., Polfa Tarchomin, przemysł farmaceutyczny, Ridgeback Biotherapeutics, Singapur, szczepienia, szczepionki, technologia, To Merck & Co.